Vědci z UTHealth Houston odhalili molekulární mechanismus, který je zodpovědný za různou závažnost infarktu v závislosti na denní době. To by mohlo otevřít cestu k inovativní léčbě, která se přizpůsobí přirozenému cirkadiánnímu rytmu. Výsledky studie byly zveřejněny v časopise Nature.
Jak denní doba ovlivňuje závažnost infarktu
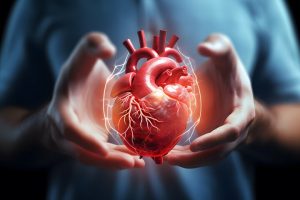
Předchozí výzkum ukázal, že závažnost poškození srdce po akutním infarktu myokardu neboli srdečním infarktu se liší v závislosti na denní době, přičemž ranní infarkty vedou k závažnějšímu poškození a horším výsledkům. Důvody těchto rozdílů však byly dříve nejasné. „Pokud proděláte infarkt ráno, je pravděpodobnější, že utrpíte fatální srdeční arytmii nebo srdeční selhání a zemřete. Položili jsme si otázku: „Proč?“,“ řekl Dr. Holger Eltzschig, PhD, hlavní autor a vedoucí a profesor oddělení anesteziologie, intenzivní péče a medicíny bolesti na McGovern Medical School UTHealth v Houstonu.
Vědci identifikovali interakci mezi dvěma proteiny, BMAL1 a HIF2A, jako klíčový faktor rozdílů v závažnosti poškození srdce po infarktu v závislosti na denní době. BMAL1 je ústředním proteinem cirkadiánního rytmu, který je zodpovědný za regulaci biologických procesů, jako jsou cykly spánek-bdění, metabolismus a uvolňování hormonů. HIF2A pomáhá tělu přizpůsobit se hypoxii – nízké hladině kyslíku – tím, že stimuluje tvorbu červených krvinek, podporuje růst nových cév a zlepšuje přežití buněk v podmínkách s nedostatkem kyslíku. k srdečnímu infarktu dochází, když je zablokován průtok krve do srdce a sval začne odumírat v důsledku nedostatku kyslíku. Vědci zjistili, že tato interakce mezi BMAL1 a HIF2A reguluje reakci myších srdečních buněk na nízkou hladinu kyslíku po infarktu, čímž moduluje reakci srdce na poškození. V preklinické studii vědci zjistili, že srdeční infarkty, ke kterým došlo kolem třetí hodiny ranní, měly za následek větší poškození srdce, včetně větší velikosti infarktu a zvýšeného rizika srdečního selhání. Srdeční infarkty, ke kterým došlo kolem třetí hodiny odpoledne, byly méně závažné a srdce se dokázalo lépe přizpůsobit nízké hladině kyslíku a podpořit účinné hojení.
Vývoj nových terapeutických strategií
Výzkum také odhalil, že proteiny BMAL1 a HIF2A se zaměřují na specifický gen, amfiregulin (AREG), který hraje důležitou roli při regulaci rozsahu poškození srdce v průběhu dne. Specifickým zacílením léků na signální dráhu BMAL1 a HIF2A-AREG se vědcům podařilo dosáhnout významné ochrany srdce, zejména pokud byla léčba načasována tak, aby se shodovala s cirkadiánní fází organismu. Podle Eltzschiga je třeba v budoucích klinických studiích zkoumat, zda načasování léčby podle vnitřních hodin těla může zlepšit výsledky u pacientů. „Tento objev otevírá nové možnosti léčby srdečních infarktů s ohledem na načasování podávání léků,“ řekl Eltzschig, který je John P. and Kathrine G. McGovern Distinguished University Chair na McGovern Medical School.
„Naše zjištění podtrhují potenciál využití cílených léků proti těmto proteinům ke snížení závažnosti srdečních záchvatů, pokud jsou podávány ve specifickou dobu. Stejně tak by pacienti podstupující operaci srdce mohli mít prospěch z takových léků, jako je aktivátor faktoru indukujícího hypoxii vadadustat, pokud by byly podány před operací.“ Výzkumný tým tvořili doktor Kuang-Lei Tsai, odborný asistent, a doktor Tao Li, postdoktorand a spoluautor, z oddělení biochemie a molekulární biologie McGovern Medical School. Pomocí kryoelektronové mikroskopie s vysokým rozlišením se jim podařilo objasnit detailní strukturní interakce mezi BMAL1 a HIF2A, což podpoří budoucí vývoj léků zaměřených na komplex BMAL1-HIF2A. Podle Eltzschiga tato práce poskytla první přímý molekulární důkaz o tvorbě jejich komplexu a přinesla důležité poznatky, které by mohly být vodítkem pro vývoj nových terapeutických strategií.