Des scientifiques de la Duke-NUS Medical School ont identifié un gène qui contrôle le comportement d’un type spécifique de macrophage cardiaque, responsable d’une cicatrisation excessive aux premiers stades des maladies cardiaques courantes, ou cardiomyopathies (diverses maladies du muscle cardiaque). Lorsque le gène appelé WWP2 (une protéine E3 ubiquitine ligase) est bloqué, la fonction cardiaque s’améliore et la formation de tissu cicatriciel ralentit la progression de l’insuffisance cardiaque.
Fonction de WWP2 dans les maladies fibrotiques
La cicatrisation ou la fibrose du cœur, comme dans les cardiomyopathies non ischémiques, est une affection progressive et un problème de santé mondial », a déclaré le professeur associé Enrico Petretto, directeur du Duke-NUS Center for Computational Biology et généticien des systèmes au sein du programme des maladies cardiovasculaires et métaboliques (CVMD) de l’école. »Dans ses premiers stades, elle se caractérise par une phase inflammatoire, de sorte qu’une intervention à ce stade pourrait retarder de manière significative la progression de la maladie »
Petretto et ses collègues de Singapour, de Chine et du Royaume-Uni étudient depuis plusieurs années la fonction de WWP2 dans les maladies fibrotiques et ont d’abord découvert qu’il s’agit d’un facteur clé de la formation de cicatrices lorsqu’il est exprimé dans les fibroblastes, les cellules qui forment le tissu cicatriciel. Dans leurs derniers résultats, publiés dans Nature Communications, l’équipe s’est intéressée aux premiers stades de la maladie.
Les macrophages exprimant WWP2 favorisent la formation de cicatrices
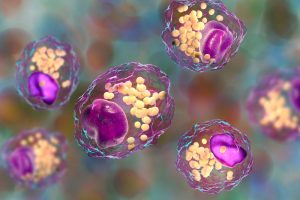
En utilisant le séquençage de l’ARN d’une seule cellule, l’équipe a découvert que lorsque la fibrose est déclenchée, une variété de macrophages différents, des cellules immunitaires qui éliminent les corps étrangers dans l’organisme, sont activés dans un modèle préclinique de maladie cardiaque. Si les macrophages sont surtout connus pour leur rôle dans l’élimination des cellules cancéreuses, des microbes et des débris cellulaires, ils contribuent également à la régénération des cellules musculaires saines.
Cependant, un sous-ensemble de ces macrophages cardiaques est contrôlé par WWP2. Ces macrophages exprimant la WWP2 favorisent activement la formation de cicatrices en incitant les cellules cardiaques locales (fibroblastes) à produire du collagène de manière incontrôlée, ce qui favorise la formation de tissu cicatriciel. Les chercheurs ont découvert que : « Lorsque WWP2 est exprimé dans les macrophages, ces cellules ‘irritent’ les fibroblastes, ce qui entraîne une cicatrisation incontrôlée. »
Une petite molécule inhibitrice bloque WWP2
En revanche, lorsque les macrophages n’expriment pas WWP2, l’équipe a observé une réduction de l’infiltration des macrophages pro-fibrotiques dans le cœur et l’effet des macrophages réparateurs a été mieux maintenu, avec des effets bénéfiques évidents sur le tissu et la fonction cardiaques dans les stades avancés de la maladie.
« Cibler WWP2, c’est comme jeter une couverture sur le feu – cela prive les flammes d’oxygène avant que toute la maison ne brûle », a expliqué le professeur Jacques Behmoaras, biologiste des systèmes du programme CVMD et co-auteur correspondant de l’étude. Bloquer la fonction de WWP2 dans ce sous-ensemble de macrophages cardiaques suffit à ralentir, voire à stopper la cicatrisation ».
L’équipe est en train de mettre au point une petite molécule inhibitrice de la WWP2 qui peut faire exactement cela. Plutôt que d’éliminer tous les macrophages sans distinction, ce qui a eu des effets délétères, l’équipe Duke-NUS cible WWP2, qui agit spécifiquement sur les macrophages pro-fibrotiques et les fibroblastes activés pour stopper la cicatrisation du cœur endommagé.
Un potentiel thérapeutique prometteur
« Comme WWP2 joue un double rôle dans la formation du tissu cicatriciel, le bloquer en freinant l’inflammation et la cicatrisation permet de faire d’une pierre deux coups. De plus, en favorisant les macrophages bénéfiques à la réparation des tissus, WWP2 devient une cible thérapeutique très attrayante.
Les chercheurs sont actuellement en train de créer de petites molécules inhibitrices ciblant une forme spécifique de la protéine WWP2, qui ont déjà montré des résultats antifibrotiques prometteurs dans les cellules. Ils estiment que cela pourrait avoir un potentiel thérapeutique pour traiter des maladies fibrotiques telles que les cardiomyopathies non ischémiques, et pourrait s’avérer efficace dans d’autres maladies fibrotiques impliquant WWP2.